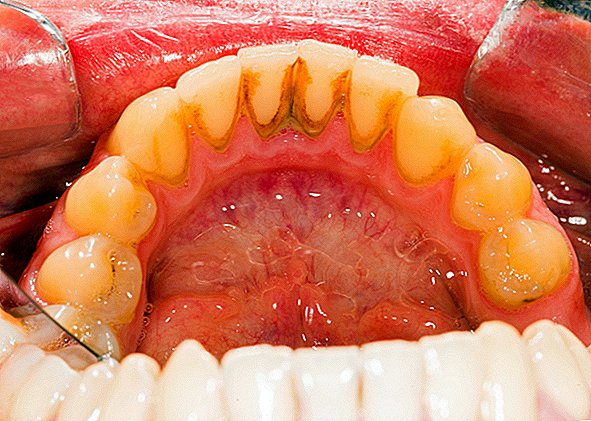
Les biofilms sont un collectif d'un ou plusieurs types de micro-organismes qui peuvent se développer sur de nombreuses surfaces différentes. Les micro-organismes qui forment les biofilms comprennent les bactéries, les champignons et les protistes.
Un exemple courant de plaque dentaire de biofilm, une accumulation visqueuse de bactéries qui se forme à la surface des dents. L'écume des étangs est un autre exemple. Des biofilms ont été trouvés poussant sur des minéraux et des métaux. Ils ont été trouvés sous l'eau, sous terre et au-dessus du sol. Ils peuvent se développer sur les tissus végétaux et animaux, et sur les dispositifs médicaux implantés tels que les cathéters et les stimulateurs cardiaques.
Chacune de ces surfaces distinctes a une caractéristique commune: elles sont humides. Ces environnements sont "périodiquement ou continuellement imprégnés d'eau", selon un article de 2007 publié dans Microbe Magazine. Les biofilms prospèrent sur des surfaces humides ou mouillées.
Les biofilms se sont implantés dans de tels environnements depuis très longtemps. Les preuves fossiles des biofilms remontent à environ 3,25 milliards d'années, selon un article de 2004 publié dans la revue Nature Reviews Microbiology. Par exemple, des biofilms ont été découverts dans les roches hydrothermales profondes de 3,2 milliards d'années du craton de Pilbara en Australie. Des biofilms similaires se trouvent dans les environnements hydrothermaux tels que les sources chaudes et les évents en eau profonde.

Formation de biofilms
La formation d'un biofilm commence lorsque des micro-organismes flottants tels que des bactéries entrent en contact avec une surface appropriée et commencent à s'enraciner, pour ainsi dire. Cette première étape de fixation se produit lorsque les micro-organismes produisent une substance gluante connue sous le nom de substance polymère extracellulaire (EPS), selon le Center for Biofilm Engineering de la Montana State University. Un EPS est un réseau de sucres, de protéines et d'acides nucléiques (comme l'ADN). Il permet aux micro-organismes d'un biofilm de coller ensemble.
L'attachement est suivi d'une période de croissance. D'autres couches de micro-organismes et d'EPS s'appuient sur les premières couches. En fin de compte, ils créent une structure 3D bulbeuse et complexe, selon le Center for Biofilm Engineering. Les canaux d'eau sillonnent les biofilms et permettent l'échange de nutriments et de déchets, selon l'article de Microbe.
De multiples conditions environnementales aident à déterminer dans quelle mesure un biofilm se développe. Ces facteurs déterminent également si elle est constituée de seulement quelques couches de cellules ou bien davantage. "Cela dépend vraiment du biofilm", a déclaré Robin Gerlach, professeur au département de génie chimique et biologique de la Montana State University-Bozeman. Par exemple, les micro-organismes qui produisent une grande quantité d'EPS peuvent se transformer en biofilms assez épais même s'ils n'ont pas accès à beaucoup de nutriments, a-t-il déclaré. En revanche, pour les micro-organismes qui dépendent de l'oxygène, la quantité disponible peut limiter leur croissance. Un autre facteur environnemental est le concept de «contrainte de cisaillement». "Si vous avez un débit très élevé à travers un biofilm, comme dans un ruisseau, le biofilm est généralement assez mince. Si vous avez un biofilm dans de l'eau qui coule lentement, comme dans un étang, il peut devenir très épais", a expliqué Gerlach.
Enfin, les cellules d'un biofilm peuvent quitter le pli et s'établir sur une nouvelle surface. Soit un amas de cellules se détache, soit des cellules individuelles éclatent du biofilm et cherchent une nouvelle maison. Ce dernier processus est connu sous le nom de «dispersion de l'ensemencement», selon le Center for Biofilm Engineering.
Pourquoi former un biofilm?
Pour les micro-organismes, vivre en tant que partie d'un biofilm présente certains avantages. "Les communautés de microbes sont généralement plus résistantes au stress", a déclaré Gerlach à Live Science. Les facteurs de stress potentiels comprennent le manque d'eau, un pH élevé ou bas ou la présence de substances toxiques pour les micro-organismes tels que les antibiotiques, les antimicrobiens ou les métaux lourds.
Il existe de nombreuses explications possibles à la robustesse des biofilms. Par exemple, le revêtement EPS gluant peut agir comme une barrière protectrice. Il peut aider à prévenir la déshydratation ou à servir de bouclier contre la lumière ultraviolette (UV). De plus, les substances nocives telles que les antimicrobiens, l'eau de javel ou les métaux sont liées ou neutralisées lorsqu'elles entrent en contact avec l'EPS. Ainsi, ils sont dilués à des concentrations qui ne sont pas mortelles bien avant de pouvoir atteindre diverses cellules profondément dans le biofilm, selon un article de 2004 dans Nature Reviews Microbiology.
Pourtant, il est possible que certains antibiotiques pénètrent dans l'EPS et traversent les couches d'un biofilm. Ici, un autre mécanisme protecteur peut entrer en jeu: la présence de bactéries physiologiquement dormantes. Pour bien fonctionner, tous les antibiotiques nécessitent un certain niveau d'activité cellulaire. Donc, si les bactéries sont physiologiquement dormantes au départ, il n'y a pas grand-chose à perturber un antibiotique.
Un autre mode de protection contre les antibiotiques est la présence de cellules bactériennes spéciales appelées «persiste». Ces bactéries ne se divisent pas et résistent à de nombreux antibiotiques. Selon un article de 2010 publié dans la revue Cold Spring Harbor Perspectives in Biology, "persiste" en produisant des substances qui bloquent les cibles des antibiotiques.
En général, les micro-organismes vivant ensemble comme un biofilm bénéficient de la présence de leurs différents membres de la communauté. Gerlach a cité l'exemple des micro-organismes autotrophes et hétérotrophes qui vivent ensemble dans des biofilms. Les autotrophes, comme les bactéries ou les algues photosynthétiques, sont capables de produire leur propre nourriture sous forme de matière organique (contenant du carbone), tandis que les hétérotrophes ne peuvent pas produire leur propre nourriture et nécessitent des sources extérieures de carbone. "Dans ces communautés multi-organismes, ils se croisent souvent", a-t-il déclaré.
Les biofilms et nous
Étant donné la vaste gamme d'environnements dans lesquels nous rencontrons des biofilms, il n'est pas surprenant qu'ils affectent de nombreux aspects de la vie humaine. Voici quelques exemples.

Santé et maladie
À mesure que la recherche a progressé au fil des ans, les biofilms - bactériens et fongiques - ont été impliqués dans diverses conditions de santé. Dans un appel de demandes de subventions de 2002, les National Institutes of Health (NIH) ont noté que les biofilms représentaient «plus de 80% des infections microbiennes dans le corps».
Les biofilms peuvent se développer sur des dispositifs médicaux implantés tels que des valves cardiaques prothétiques, des prothèses articulaires, des cathéters et des stimulateurs cardiaques. Cela entraîne à son tour des infections. Le phénomène a été observé pour la première fois dans les années 80 lorsque des biofilms bactériens ont été découverts sur des cathéters intraveineux et des stimulateurs cardiaques. Les biofilms bactériens sont également connus pour provoquer une endocardite infectieuse et une pneumonie chez les personnes atteintes de mucoviscidose, selon l'article de 2004 dans Nature Reviews Microbiology, entre autres infections.
"La raison pour laquelle la formation de biofilms est une grande source de préoccupation est que, dans un biofilm, les bactéries sont plus résistantes aux antibiotiques et autres désinfectants majeurs que vous pourriez utiliser pour les contrôler", a déclaré AC Matin, professeur de microbiologie et d'immunologie à Stanford. Université. En fait, par rapport aux bactéries flottantes, celles qui se développent sous forme de biofilm peuvent être jusqu'à 1 500 fois plus résistantes aux antibiotiques et autres agents biologiques et chimiques, selon l'article de Microbe. Matin a décrit la résistance au biofilm combinée à l'augmentation générale de la résistance aux antibiotiques chez les bactéries comme un «double coup dur» et un défi majeur pour le traitement des infections.
Les biofilms fongiques peuvent également provoquer des infections en se développant sur des dispositifs implantés. Espèces de levures telles que les membres du genre Candidose croître sur les implants mammaires, les stimulateurs cardiaques et les valves cardiaques prothétiques selon un article de 2014 publié dans la revue Cold Spring Harbor Perspectives in Medicine. Candidose les espèces se développent également sur les tissus du corps humain, entraînant des maladies telles que la vaginite (inflammation du vagin) et la candidose oropharyngée (une infection à levures qui se développe dans la bouche ou la gorge). Cependant, les auteurs notent que la résistance aux médicaments n'a pas été montrée dans ces cas.
Bioremédiation
Parfois, les biofilms sont utiles. "La biorestauration, en général, consiste à utiliser des organismes vivants ou leurs produits - par exemple, des enzymes - pour traiter ou dégrader des composés nocifs", a déclaré Gerlach. Il a noté que les biofilms sont utilisés dans le traitement des eaux usées, des contaminants de métaux lourds comme le chromate, des explosifs comme le TNT et des substances radioactives comme l'uranium. "Les microbes peuvent soit les dégrader, soit modifier leur mobilité ou leur état toxique et donc les rendre moins nocifs pour l'environnement et pour l'homme", a-t-il déclaré.
La nitrification à l'aide de biofilms est une forme de traitement des eaux usées. Pendant la nitrification, l'ammoniac est converti en nitrites et nitrates par oxydation. Cela peut être fait par des bactéries autotrophes, qui se développent sous forme de biofilms sur des surfaces en plastique, selon un article de 2013 publié dans la revue Water Research. Ces surfaces en plastique ne mesurent que quelques centimètres et sont réparties dans toute l'eau.
Le TNT explosif (2,4,6-trinitrotoluène) est considéré comme un polluant du sol, des eaux de surface et des eaux souterraines. La structure chimique du TNT est constituée de benzène (un cycle aromatique hexagonal composé de six atomes de carbone) attaché à trois groupes nitro (NO2) et un groupe méthyle (CH3). Les microorganismes dégradent le TNT par réduction, selon un article de 2007 publié dans la revue Applied and Environmental Microbiology. La plupart des micro-organismes réduisent les trois groupes nitro, tandis que certains attaquent l'anneau aromatique. Les chercheurs - Ayrat Ziganshin, Robin Gerlach et ses collègues - ont découvert que la souche de levure Yarrowia lipolytica a été en mesure de dégrader le TNT par les deux méthodes, mais principalement en attaquant l'anneau aromatique.
Piles à combustible microbiennes
Les piles à combustible microbiennes utilisent des bactéries pour convertir les déchets organiques en électricité. Les microbes vivent à la surface d'une électrode et y transfèrent des électrons, créant finalement un courant, a déclaré Gerlach. Un article publié en 2011 dans Illumin, un magazine en ligne de l'Université de Californie du Sud, note que les bactéries qui alimentent les piles à combustible microbiennes décomposent les aliments et les déchets corporels. Cela fournit une source d'énergie à faible coût et une énergie propre et durable.
Recherche en cours
Notre monde regorge de biofilms. En fait, au milieu du 20e siècle, plus de bactéries ont été trouvées sur les surfaces intérieures des conteneurs contenant des cultures bactériennes, que flottant librement dans la culture liquide elle-même, selon l'article de 2004 dans Nature Reviews Microbiology. La compréhension de ces structures microbiennes complexes est un domaine de recherche actif.
"Les biofilms sont des communautés incroyables. Certaines personnes les ont comparés à des organismes multicellulaires parce qu'il y a beaucoup d'interactions entre les cellules individuelles", a déclaré Gerlach. "Nous continuons à en apprendre davantage à leur sujet, et nous continuons à apprendre comment mieux les contrôler; à la fois pour un préjudice réduit, comme dans le domaine de la médecine, ou pour un bénéfice accru comme dans la biorestauration. Nous n'allons pas manquer de des questions intéressantes dans ce domaine. "